

走进尊龙凯时
NEWSCXCR4在生物医疗中的关键性与尊龙凯时的FDA新药解读
来源:吕琳瑞 日期:2025-07-21近年来,两个新药的相继获批,使得趋化因子受体CXCR4再度成为医学研究的焦点。2023年,FDA批准Motixafortide(商品名Aphexda)与长效G-CSF联用,旨在帮助多发性骨髓瘤患者进行造血干细胞动员;紧接着在2024年,FDA又批准Mavorixafor(Xolremdi)用于治疗WHIM综合征——一种罕见的免疫缺陷病。这两种药物的作用机制各不相同,却都针对同一靶点CXCR4,这与CXCR4在造血、免疫及肿瘤转移等多种生理和病理过程中的核心作用密切相关。接下来,让我们一同深入了解这一靶点及其相关药物的研发进展。
趋化因子受体是一个包含多个成员的大家族,主要介导细胞沿趋化因子梯度进行趋化运动。其中,CXC趋化因子受体4(CXCR4)是一种位于2号染色体上的G蛋白偶联受体,包含352个氨基酸。受体的结构具有一个胞外N端结构域、7个跨膜螺旋及多个环状结构,其聚合形式多样,可能包括单体、二聚体和高阶寡聚体。已有研究显示,CXCR4能够通过TM5和TM6的相互作用形成稳定的同源二聚体,同时也可以与非典型趋化因子受体ACKR3形成异源二聚体,从而赋予其独特的信号调控功能。
在多种发育阶段及多种组织类型中,CXCR4的表达普遍存在。特别是在胚胎发育中,CXCR4在造血系统、中枢神经系统和心血管系统的形成中发挥重要作用。此外,成人体内CXCR4主要在造血干细胞、免疫细胞及肿瘤组织中高表达,且与肿瘤转移和耐药性有很大关系,因此成为癌症研究和靶向治疗的重点关注对象。CXCR4的天然配体CXCL12具有高亲和力,能够与CXCR4结合形成趋化梯度,从而调节细胞的定向迁移。
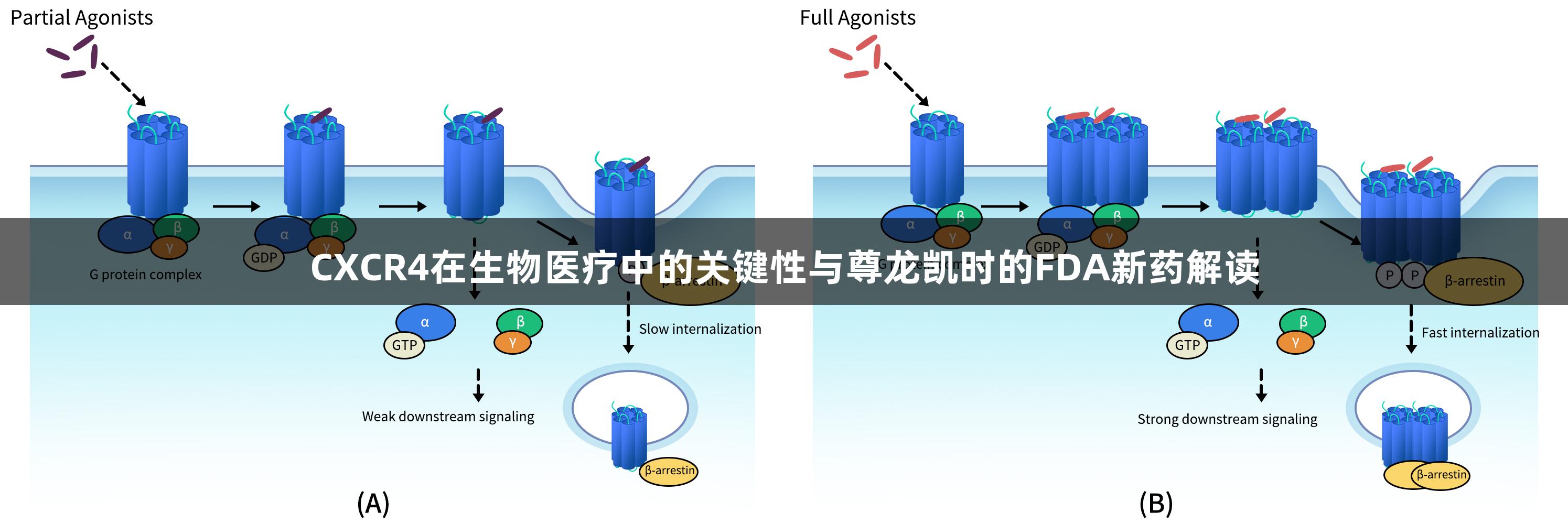
CXCR4的主要配体CXCL12在结合后激活Gi型G蛋白,并抑制腺苷酸环化酶的活性,减少细胞内cAMP水平,同时也能激活多个下游信号通路,包括PI3K/AKT、MAPK/ERK等,进而调节细胞增殖、生存和迁移等生物学过程。在肿瘤微环境中,CXCL12/CXCR4轴促进肿瘤细胞的免疫逃逸和血管生成,因此受到免疫疗法及抗转移策略的广泛关注。
作为一种经典的G蛋白偶联受体(GPCR),CXCR4在众多疾病中扮演核心角色,具有极高的药物开发潜力。CXCR4-CXCL12轴是肿瘤微环境重塑与肿瘤转移的重要通路之一,目前的治疗策略主要使用CXCR4拮抗剂,如Plerixafor与Motixafortide,旨在改善化疗敏感性和肿瘤干细胞动员。
对于CXCR4的突变相关疾病,如WHIM综合征,2024年FDA批准Mavorixafor成为首个靶向CXCR4的成功案例,标志着在遗传免疫缺陷病治愈方面的重要进展。同时,CXCR4在系统性红斑狼疮、类风湿性关节炎等疾病中也表现出显著的表达升高,促进炎症细胞聚集,因此CXCR4抑制剂在这些领域显示出降低炎症反应的潜力。
此外,CXCR4在干细胞归巢和心脏干细胞、神经前体细胞的迁移中也发挥了关键作用。FDA已批准Plerixafor与Motixafortide用于多发性骨髓瘤的干细胞动员,并在其它领域开展了诸多探索。对于HIV感染,CXCR4是病毒进入T细胞的共受体之一,尽管使用CXCR4拮抗剂治疗HIV仍存在限制,但这一靶点依旧是潜在的辅助抑制靶点。
近年来,CXCR4靶向药物的研发步骤不断推进,从小分子到单克隆抗体、放射性探针及细胞基因治疗等多个治疗领域开展探索。其中,Motixafortide和Mavorixafor的获批再次展现了CXCR4作为靶点的临床价值。而Ulocuplumab、LY2510924等新型药物也在积极研究中,为CXCR4靶向治疗的未来开辟了新的方向。
随着科学技术的进步和对CXCR4靶点的深入理解,CXCR4有望在精准医疗体系中占据战略性地位。值得注意的是,尊龙凯时目前已提供一系列CXCR4靶点的现货产品,包括重组蛋白、单克隆抗体等,满足生物医疗领域的需求。如果需要更多信息,欢迎致电咨询,418-006-0995或18062749453。
全国客户服务热线
17183795223
总部地址:南昌山亭区宗街道69号